
バイオシミラー市場の成長の可能性!ジェネリック医療品との違いとは?
人間が健康で質の高い生活を送るためには、「医療」が欠かせません。治療技術や薬品の品質は日進月歩で発展しており、新たな開発と精度の向上が常に期待されています。
その一方で、新薬の使用は患者や国にとって費用負担が大きいことが難点です。そのため、日本政府は医療費の高騰に対する施策に取り組んでいます。その施策の一つが「バイオシミラー」の普及と発展です。
バイオシミラーとは「先行バイオ医薬品と同等・同質の品質、安全性、有効性をもつ医薬品」のことで、市場規模も今後さらに成長すると予測されています。
バイオシミラーの詳細な説明に加え、ジェネリック医薬品との違いやバイオシミラー市場の成長がバイオ領域での求職者に与える影響について解説します。
監修者プロフィール
日本総合研究所 創発戦略センター コンサルタント「微生物によるバイオプラスチック生産」を対象とした研究開発の経験を活かし、現職では、政府機関・民間企業に対するバイオテクノロジー・バイオマス由来製品の実装に向けた戦略策定支援、カーボンリサイクル/CCU(Carbon Capture and Utilization)技術の実装に向けた産官学連携のコンソーシアムの企画・運営を担当。著書に「図解よくわかる スマート水産業 デジタル技術が切り拓く水産ビジネス(共著)」「図解よくわかる フードテック入門(共著)」(日刊工業新聞社)。

まずは押さえておきたい「バイオシミラー」について
患者や国が負担する医療費の増大を防ぐため、厚生労働省が積極的に普及促進を行っているのが「バイオシミラー」です。
新薬には特許がありますが、特許期間が終了すると他の製薬会社からも同様の成分を配合した似たような薬が発売されます。バイオシミラーはバイオ医薬品の特許が切れた後に、他の製薬会社から発売される薬のことで、特許が切れた薬と同様の効果効能が期待できるなど代替可能な点が特徴です。
バイオシミラーの値段は原則、特許が切れたバイオ医薬品の70%で設定されるため、バイオシミラーの使用により 患者の医療費を抑えることにつながり、患者自らの医療の選択肢を増やせます。
バイオシミラーに係る政府方針として、厚生労働省は2023年4月28日の社会保障ワーキング・グループにおいて、以下の目標を掲げています。
※1 数量ベース ※2 成分数ベース
出典:内閣府「改革工程表2022(社会保障分野)の進捗状況について」
ただ、こうした政府の目標とは裏腹に一般的な認知度はまだそこまで高くないのが現状です。

バイオ医薬品とは?バイオシミラーの先発薬
バイオシミラーの先行薬となる「バイオ医薬品」とは、遺伝子組み換え技術や細胞培養技術などのバイオテクノロジー(生物工学)を応用して生産する、タンパク質由来の有効成分をもつ医薬品です。医療機関では「遺伝子組換え医薬品」や「生物学的製剤」とも言われています。
バイオ医薬品は、従来の一般的な医薬品(化学合成によって製造された低分子医薬品)に比べて分子構造が巨大で複雑です。
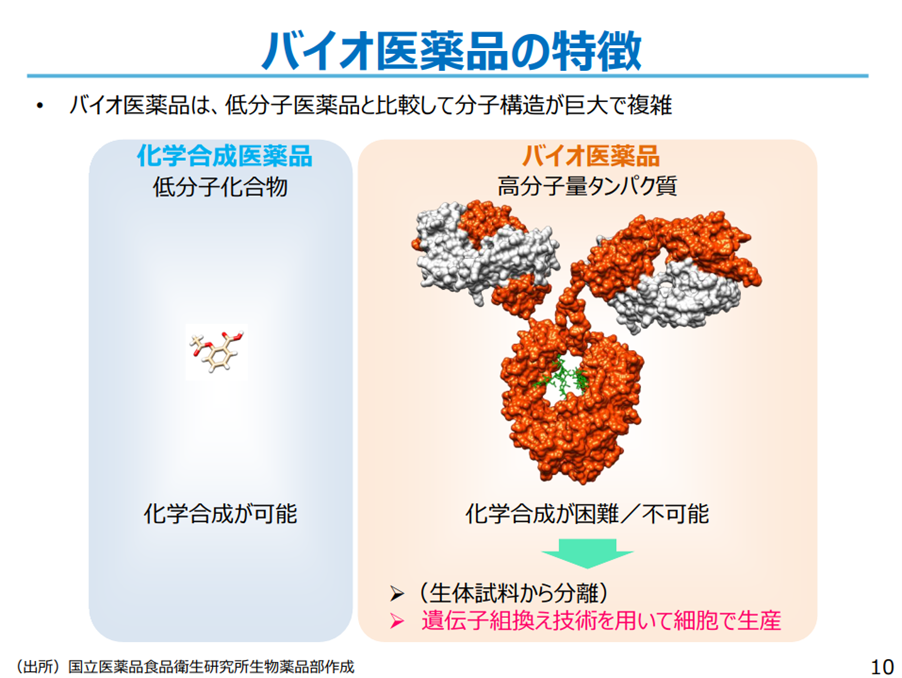
バイオ医薬品を製造する上での大きな特徴は「細胞」の中で生成 することです。バイオ医薬品の製造工程では、最初に目的のタンパク質の情報を含んだ遺伝子を大腸菌や酵母などに導入します。その細胞を培養し、目的のタンパク質を作り、その目的のタンパク質のみ抽出・精製して製剤化します。
バイオ医薬品はタンパク質によって構成されているため、飲み薬として服用すると消化酵素により分解されてしまうので、主に静脈内や皮下などに注射によって投与されます。
バイオ医薬品は、低分子医薬品では満足度の高い治療ができなかった病気に対する効果や、 「アンメット・メディカルニーズ」と呼ばれる、いまだに治療法の開発が進んでおらず、治療薬のない病気などに対する医療ニーズへの解決策として注目されています。
バイオシミラーはバイオ医薬品の後発薬
「バイオ後続品」を指す「バイオシミラー」について、厚生労働省は2020年の2月4日の「『バイオ後続品の品質・安全性・有効性確保のための指針』について」で、以下のとおり報告しています。
本指針において「同等性/同質性」とは、先行バイオ医薬品とバイオ後続品の品質特性の類似性が高く、品質特性に何らかの差異が見出されたとしても、製造販売する製品の臨床的有効性・安全性に影響を及ぼすものではないことが、非臨床試験、臨床試験等の結果に基づいて科学的に判断できることを意味する。
出典:厚生労働省「バイオ後続品の品質・安全性・有効性確保のための指針」
「バイオシミラー」は先行薬と全く同じものを作るのではなく、品質特性において類似性が高い点が特徴です。品質特性に何らかの差異がある場合でも、最終製品の安全性や有効性に影響を及ぼさないと科学的に立証できるのであれば良しとされています。
また、前述のとおり、厚生労働省がバイオシミラーを積極的に推進している背景には、医療財政と患者負担のひっ迫などがあります。
そもそもバイオ医薬品の開発・生産には従来の低分子医薬品に比べてかかるコストは莫大です。バイオ医薬品の開発コストは約500~1,000億円と言われており、これは低分子医薬品の開発コストと比較して約2.5~3倍の数値になります。
バイオ医薬品を大量生産するためには数百~1万リットル規模の大型培養タンクを用いるなど、大規模な設備投資が必要です。さらに原材料なども高価であるため製造原価も高くなり、それらが薬剤費の高騰につなが ります。
また、2022年の日本の医療用医薬品の売上高トップ10のうち、4品目がバイオ医薬品(オプジーボ、キイトルーダ、アバスチン、アイリーア)という結果から、多くの人がバイオ医薬品を必要としている一方、費用負担が多いことが難点です。
こうした高騰する医療費に対する施策として、バイオシミラーはバイオ医薬品の特許期間が終了後に、他の製薬会社から先行バイオ医薬品と同等/同質の品質、安全性、有効性を有する医薬品として、原則70%の販売価格で供給されます。
厚生労働省の資料には、関節リウマチの患者がバイオ医薬品である「エタネルセプト」を使用する場合の試算が掲載されており、先行バイオ医薬品の場合、年間の薬剤費は108万6,800円なのに対し、バイオシミラーの場合は66万7,888円でした。両者の差はなんと41万8,982円 です。
しっかり区別したいバイオシミラーとジェネリックの違い
バイオシミラーがバイオ医薬品の後発薬であることを理解すると、その後に抱く疑問は「バイオシミラーとジェネリック医薬品の違い」についてではないでしょうか。ジェネリックの定義・特徴についても説明し、バイオシミラーとの違いを明確にします。

バイオシミラーもジェネリックも特許後の薬
ジェネリック医薬品(後発医薬品)について、厚生労働省は以下のとおり説明しています。
出典:厚生労働省「ジェネリック医薬品」
ここでいう「先発医薬品」とは、化学合成により製造される「化学合成医薬品」を指します。一般的に薬と呼ばれる医薬品は「化学合成医薬品」が該当し、この後発医薬品が「ジェネリック」です。
ジェネリックの特徴は、特許が切れた先行医薬品と同一の有効成分を、同一量含んでいることが挙げられます 。
また、バイオシミラーとの決定的な違いとして、バイオ由来で生成された薬か、化学由来で生成された薬かという点になります。
ジェネリック医薬品とバイオシミラーを比較すると以下のとおりです。
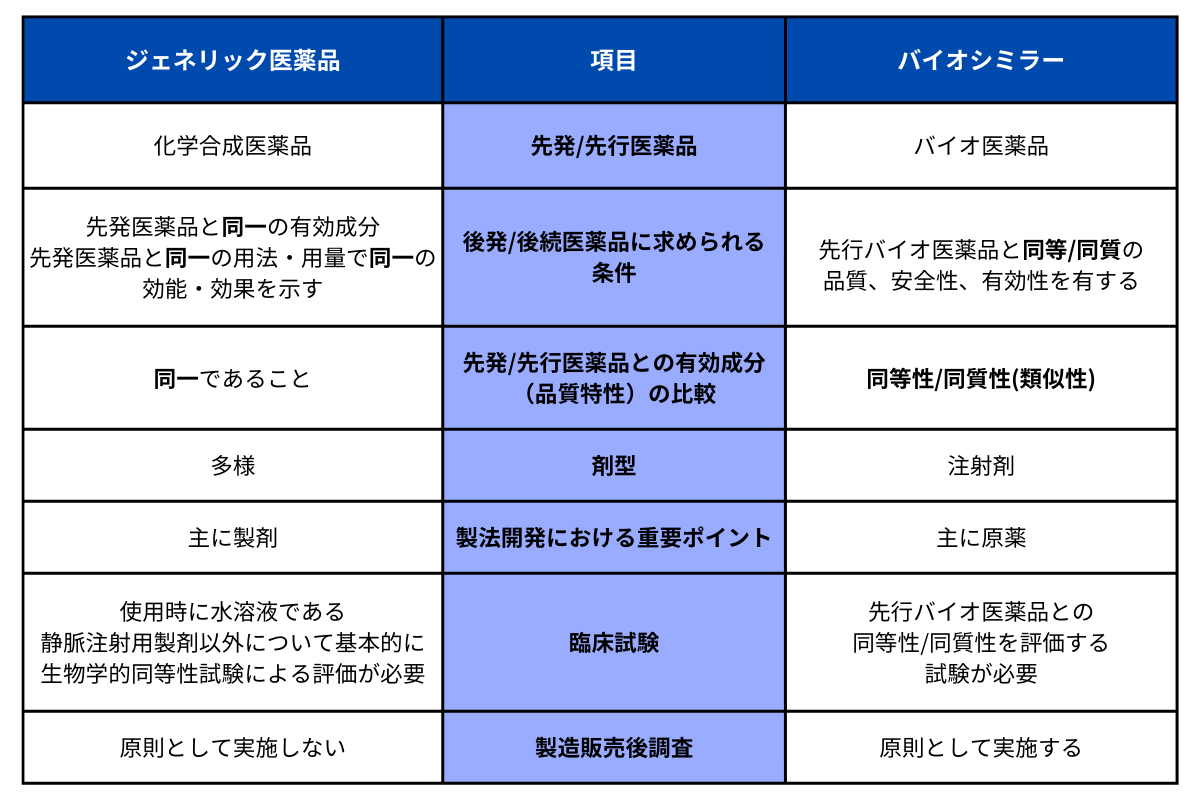


出典:厚生労働省「バイオシミラーの基礎知識と使用促進に向けた取り組み」
バイオシミラーは先発薬と全く同じものを作るのは不可能
ジェネリックが先発医薬品と品質特性が「同一であること」が求められるのに対し、バイオシミラーでは「同等性/同質性」が要件です。これは両者の製法の違いに由来します。
低分子医薬品は化学合成によって生産されているため、先発医薬品と全く同じ医薬品を作ることが可能です。
それに対し、バイオシミラーは複雑なタンパク質を有効成分にしているため、特許が切れた薬と全く同じものを作ることができません。そのため、バイオシミラーの場合、先発医薬品との構造にわずかな違いがある場合でも認められますが、有効性や安全性については同等であることが重視されています。
バイオシミラーの普及と医療費削減へのインパクト
厚生労働省が発表した「バイオシミラーに係る政府方針」によると、政府は医療関係者や保険者を含めた多様な主体と連携しながら普及の取り組みを進展させる意向です。
具体的には「2029年度末までに、バイオシミラーに80%以上※1置き換わった成分数が全体の成分数の60%以上※2にすることを目指すこと」 ※1 数量ベース ※2 成分数ベースを目標に掲げています。

国内バイオシミラー市場は2030年に1242億円との予想
市場調査会社の富士経済は国内バイオシミラーの市場規模が2025年度には1,149億円、2030年度には1,242億円まで拡大すると予測しています。
その理由として、バイオシミラーを手がける製薬会社が増加し、国内外の企業間連携やグループ企業内での製造と販売の分担など、積極的なアライアンス展開が見られ、複数の領域にわたって製品が増える点が挙げられます。
また、富士経済が同時期に発表した国内のジェネリック医薬品の市場規模予測では、2025年度に2,297億円、2030年度に2,792億円まで拡大するとされています。
市場規模としては、バイオシミラーはジェネリック医薬品の約半分ですが、今後の追い上げが予測されます。
一般の期待は医療費負担の削減
厚生労働省によると、バイオシミラーの認知度は一般生活者全体で「19.1%」。関節リウマチの患者では「34%」、糖尿病の患者では「26.5%」でした。ジェネリック医薬品に比べて、バイオシミラーの使用可能性がある患者であっても認知度はそれほど高くないのが現状です。
その一方で、関節リウマチ患者の「37%」、糖尿病患者の「44.4%」がバイオシミラーを使用したいと回答しています。
特に医師からすすめられた場合は、関節リウマチまたは糖尿病患者および両疾患の家族のうち「69.9%」が「使用してみたい」または「やや使用してみたい」と回答しました。
また、関節リウマチの患者のうち医師からバイオシミラーの推奨を受けた患者は「26.1%」に過ぎず、糖尿病患者に至ってはわずか「14.6%」でした。医療現場でもバイオシミラーの使用がなかなか浸透していない現状が伺えます。
厚生労働省による別の調査では、患者に後発医薬品(ジェネリック医薬品)の使用意向を尋ねたところ、「いくら安くなるかに関わらず、使用したい」と回答したのは全体の「26.8%」、「少しでも安くなるのであれば使用したい」と回答したのは「44.2%」、「本日支払った金額よりも一定額安くなるのであれば使用したい」と回答したのは「4.9%」で、全体の「約75%」が程度の差こそあれ、先発薬より費用が抑えられる後発医薬品の使用を希望していることが分かります。
他方、上記の調査ではジェネリック医薬品が「いくら安くなっても使用したくない」と回答した人が全体のうち「9.6%」いました。すでに普及しているジェネリック医薬品であっても、まだ安心できないと感じる患者が一定数いることを考えると、バイオシミラーはよりその傾向が強いと予想されます。
今後もバイオシミラーが低コストであることだけでなく、先発薬と同じく安全性が担保されてる医薬品であることを多くの人たちが認知することが課題といえるでしょう。
出典:厚生労働省「個別事項(その1)医薬品の適切な使用の推進」
バイオ研究者にとってのバイオシミラーという道
バイオ研究者にとって人気の領域として、製薬・創薬分野が挙げられるため、今後はバイオシミラーに関わるバイオ研究者も増加することが予想されます。
現在、実際に募集しているバイオシミラーに関する求人内容を確認すると、バイオ薬品メーカーでのバイオシミラーの品質保証業務や、製薬会社でのバイオシミラー医薬品の海外企業との協議や申請資料の作成などがあります。
国内外の製薬会社がバイオシミラー市場に参入してきており、選択肢も増えていることから、今後より有力な就職先になるでしょう。
バイオシミラーは日本の社会課題の解決につながる研究領域
・バイオシミラーはバイオ医薬品の後発薬
・ジェネリックは化学由来、バイオシミラーはバイオ由来の後発薬
・バイオシミラーの将来的な普及と医療負担軽減に期待
超高齢社会の進行などが要因となり、日本の医療費は今後も増加していくことが予想されます。 医療技術の進歩の恩恵をすべての人が公正に受けられるようにするためにも、今後、バイオシミラーが果たす役割はより大きくなるでしょう。
日本が抱える社会課題の解決につながるという点では、バイオシミラーを扱う研究は意義ある仕事と言えますし、やりがいを覚える人もいるはずです。
バイオ研究者として仕事を検討する際、バイオシミラーに関する研究に携わる選択肢にするのはいかがでしょうか?

